Minęło sporo czasu od ostatniego wpisu poświęconego izotopom i prowadzonym przeze mnie badaniom. Trochę się w tej materii działo, głównie za sprawą materii organicznej makrofitów. We wcześniejszych wpisach wspominałem, że prowadzę projekt naukowy ukierunkowany na badanie jezior lobeliowych i sygnału izotopowego makrofitów, też tych specyficznych dla tego typu jezior, tj. izoetydów czyli roślin tworzących rozety, zimozielonych o znacznym systemie korzeniowym, wymagających niskiej trofii, czyli małożyznych wód i osadów. Z tych powodów rośliny te wyspecjalizowały się w takich środowiskach i potrafią je zdominować. Dlatego, dobrze zachowanym jeziorem lobeliowymi jest jezioro o niskim przewodnictwie elektrolitycznym, niskim stężeniu jonów wapnia oraz niskim niskich stężeniach biogenów. Ważne jest niskie stężenie fosforu, który w tych jeziorach najczęściej jest czynnikiem limitującym rozwój roślinności, zwłaszcza tej naczyniowej, zanurzonej w wodzie. Choć też tego typu roślinność dość często w takich jeziorach występuje lecz nie w takim zagęszczeniu jak w jeziorach bardziej żyznych. Tu chciałbym odesłać do opisu projektu na stronie Narodowego Centrum Nauki. Udało mi się już opublikować znaczną część materiału z tego projektu i go rozliczyć, z czego się niezmiernie cieszę, gdyż jego realizacja przypadła na okres pandemii koronawirusa, co dość znaczącą wpłynęło na jego planowany harmonogram. W tym czasie udało mi się pozyskać dodatkowe środki na analizy izotopowe pokaźnego zbioru materiałów zielnikowych kolegów z Katedry Ekologii Roślin Uniwersytetu Gdańskiego, gdzie „o zgrozo” już od prawie 6 lat pracuję. Dzięki temu rozszerzyłem swoją bazę danych izotopowych o materiał z jezior twardowodnych (znacznie wyższe ilość soli rozpuszczonych w wodzie i wyższe stężenie jonów wapnia w stosunku do miękkowodnych jezior lobeliowych) i rzek północnej Polski. Pozwoliło to na, moim zdaniem, ciekawe badania porównawcze oraz umożliwiło skupienie się na kolejnym gradiencie środowiskowym tj. wpływie zróżnicowanego użytkowania terenu na sygnał izotopowy makrofitów zanurzonych rzek północnej Polski. Znaczną część tych badań prezentowałem na różnych konferencjach ogólnopolskich i międzynarodowych, zachęcając również moje dyplomantki do przygotowania posterów i prezentowania samodzielnie ciekawych wyników badań. Jeśli ktoś jest mocno zainteresowany szczegółami tych doniesień konferencyjnych oraz trzech prac, które powstały na bazie materiałów z rzek i jezior twardowodnych to znajdziecie je na mim profilu na ResearchGate lub Bazie Wiedzy Uniwersytetu Gdańskiego.
Przechodząc do odpowiedzi na pytanie (Rycina 1) stanowiące tytuł tego wpisu oraz silnie nawiązuje do mojego ostatniego wystąpienia konferencyjnego na XXVI Zjeździe Hydrobiologów Polskich chciałbym zaznaczyć, iż typ ekosystemu wodnego znacząco determinuje skład izotopowych węgla oraz azotu makrofitów.
Rycina 1. Jak typ ekosystemu determinuje skład stabilnych izotopów węgla i azotu w materii organicznej zanurzonej roślinności wodnej?
Zestawiając z sobą posiadane wyniki z jezior miękkowodnych (lobeliowych ale w znacznym gradiencie pH oraz żyzności), twardowodnych (od czystych ramienicowych przez wzorcowe jeziora rdestnicowe do jezior silnie eutroficznych) oraz z rzek (i stanowisk ze zlewni leśnych, rolniczych i bardziej zurbanizowanych) dla sygnatur izotopowych węgla wykazano istotne zróżnicowanie (Rycina 2). Najwyższe wartości notowano w jeziorach twardowodnych, później w miękkowodnych a najniższe w rzekach (Rycina 2). Głównie jest to spowodowane innym chemizmem i zróżnicowaną dostępnością nieorganicznego węgla rozpuszczonego w wodzie w postaci CO2 i HCO3–. Formy te różnią się o 7-12‰ co wyjaśnia część obserwowanych różnic. Reszta może mieć inne podłoże tj. większy udział 12C w puli węgla nieorganicznego pochodząca z szybko mineralizującej się materii organicznej w rzekach w porównaniu z jeziorami, zwłaszcza w ich głębszych nie mieszających się często partiach. Pośrednie wyniki dla jezior lobeliowych związane są z tym, iż w tym zestawieniu danych są też rośliny z grupy izoetydów i mchy, które cechują się niższymi wartościami gdyż muszą korzystać tylko z CO2 a ponadto izoetydy z CO2 z osadów, który powinien cechować się niskimi wartościami sygnatury izotopowej. Ewidentnie zatem widać, iż to ekosystem wodny w dużym stopniu determinuje skład izotopowy zanurzonych roślin wodnych. Tu też chciałbym przypomnieć wpis o Stuckenia pectinata w krótkim gradiencie zasolenia, tam też typ ekosystemu wodnego determinowała wartości sygnatur izotopowych węgla. Wraz ze wzrostem zasolenia wartości izotopowe liści i łodyg wzrastały i były dość wysokie w najbardziej zasolonych zatokach.
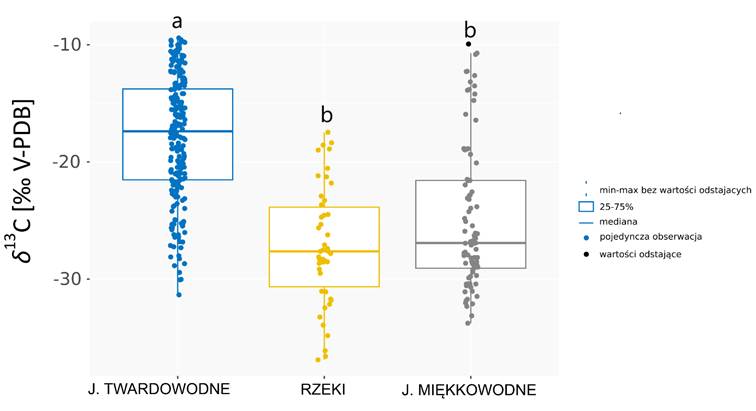
Rycina 2. Porównanie wartości δ13C trzech badanych typów ekosystemów słodkowodnych. Inne litery nad wykresami oznaczaj różnice statystycznie istotne, sprawdzone za pomocą testu post hoc Dunna z (p < 0,05)
O ile sygnał węglowy w dużej mierze odzwierciedla dostępność form nieorganicznego węgla, o tyle wartości δ15N są bardziej czułe na wpływy zewnętrzne – zwłaszcza zanieczyszczenia pochodzenia antropogenicznego.
Analizy statystyczne wykazały, że sygnatury izotopowe azotu makrofitów z odmiennych typy ekosystemów różnią się między sobą (Rycina 3). W tym przypadku chodzi bardziej o to narażenie na dopływ ścieków bytowych i spływów powierzchniowych wody z pól, gdzie stosuje się nawozy naturalne pochodzenia zwierzęcego. Pisałem więcej o tym na blogu Świat Wody, co możecie sprawdzić tu. Dopływ tego typu zanieczyszczeń na większą skalę wpływa na makrofity w rzekach gdzie ten dopływ rejestrowany jest przez makrofity poprzez wysokie wartości sygnatury izotopowej azotu (Rycina 3). W jeziorach miękkowodnych (lobeliowych) te zróżnicowanie może być spowodowane odmiennym chemizmem wód w stosunku do jezior twardowodnych, co też może wpływać na inne mechanizmy występowania procesów nitryfikacji i denitryfikacji. Ten aspekt wymaga jednak dalszych szczegółowych badań z uwzględnieniem pętli mikrobiologicznej. Może w przyszłości nawiąże jakąś współpracę by to bardziej rozpracować.

Rycina 3. Porównanie wartości δ15N trzech badanych typów ekosystemów słodkowodnych. Inne litery nad wykresami oznaczaj różnice statystycznie istotne, sprawdzone za pomocą testu post hoc Dunna (p < 0,05).
Podsumowując, wydaje mi się, iż można śmiało powiedzieć, że typ ekosystemu determinuje w znacznym stopniu sygnał izotopowy makrofitów. Ponadto zróżnicowanie sygnatur izotopowych makrofitów może zatem stanowić użyteczne narzędzie diagnostyczne przy ocenie stanu troficznego ekosystemów wodnych. Jeżeli interesują was bardziej szczegóły to zapraszam do lektury naszych publikacji. Ostrzegam jednak, że to lektura wymagająca cierpliwości.
Literatura:
Guo H.R., Wu Y., Hu C.C. & Liu X.Y. (2022). Elevated Nitrate Preference Over Ammonium in Aquatic Plants by Nitrogen Loadings in a City River. Journal of Geophysical Research: Biogeosciences 127, 1–14. https://doi.org/10.1029/2021JG006614
Guo Q., Wang C., Wei R., Zhu G., Cui M. & Okolic C.P. (2020). Qualitative and quantitative analysis of source for organic carbon and nitrogen in sediments of rivers and lakes based on stable isotopes. Ecotoxicology and Environmental Safety 195, 110436. https://doi.org/10.1016/j.ecoenv.2020.110436
Pronin E. (2024). The Possible Use of Stable Carbon and Nitrogen Isotope Signal and Spectral Analysis to Identify Habitat Condition of Aquatic Plants. Limnological Review 24, 17–29. https://doi.org/10.3390/limnolrev24010002
Pronin E., Banaś K., Chmara R., Ronowski R., Merdalski M., Santoni A.-L., et al. (2024). Characteristics of Stable Carbon and Nitrogen Isotopes in Different Ecological Plant Groups and Sediments Collected from 14 Softwater Lakes in Poland. Water (Switzerland) 16, 3403. https://doi.org/https://doi.org/10.3390/w16233403
Pronin E., Banaś K., Chmara R., Ronowski R., Merdalski M., Santoni A.-L., et al. (2023). Do stable carbon and nitrogen isotope values of Nitella flexilis differ between softwater and hardwater lakes? Aquatic Sciences 85, 79. https://doi.org/10.1007/s00027-023-00976-6
Pronin E., Panettieri M., Torn K. & Rumpel C. (2019). Stable carbon isotopic composition of dissolved inorganic carbon (DIC) as a driving factor of aquatic plants organic matter build-up related to salinity. Ecological Indicators 99, 230–239. https://doi.org/10.1016/j.ecolind.2018.12.036
Pronin E., Wrosz Z., Banaś K. & Merdalski M. (2025). Following the Footsteps of macrophytes: Potential application of isotope signals in pollution monitoring: A case study of northern Polish rivers. Ecohydrology & Hydrobiology, 100650. https://doi.org/10.1016/j.ecohyd.2025.100650
Wrosz Z., Banaś K., Merdalski M. & Pronin E. (2025). Stable Carbon and Nitrogen Isotope Signatures in Three Pondweed Species—A Case Study of Rivers and Lakes in Northern Poland. Plants 14, 2261. https://doi.org/10.3390/plants14152261
