W ostatnim wpisie napomniałem, że w obecnie realizowanym projekcie naukowym finansowanym przez Narodowe Centrum Nauki w Krakowie (NCN Nr 2019/32/C/NZ8/0014), zajmuje się zgoła innymi rzeczami niż jakość wody w kąpieliskach. W projekcie staram się wraz z zespołem przebadać środowisko jeziorne używając metod związanych ze składem stabilnych izotopów. W tym wpisie omówię czym są i jak można zastosować stabilne izotopy. Jeżeli jesteście ciekawi to odsyłam do popularnonaukowego opisu projektu oraz śledzenia kolejnych wpisów.
W przyrodzie mamy dwa rodzaje izotopów: stabilne – to znaczy stałe, które nie rozpadają się na inne pierwiastki lub nie przekształcają się w pierwiastki z mniejszą ilością neutronów w jądrze komórkowym w czasie. Drugie, to te niestabilne i często z tego powodu promieniotwórcze, które zazwyczaj po rozpadzie stają się innym pierwiastkiem chemicznym. Te drugie są bardziej znane z uwagi na fakt wykorzystywania ich np. do określania wieku skał, czyli datowania, czy też w elektrowniach atomowych.

Zdecydowanie mniej popularne i zdecydowanie mniej „medialne” są izotopy stabilne.
Izotopy to różne formy tego samego pierwiastka chemicznego, które mają taką samą liczbę protonów a różnią się miedzy sobą liczbą neutronów w jądrze atomowym. Istnieje wiele pierwiastków, które mają izotopy stabilne. Najbardziej popularnym i znanym ze szkolnych ław jest wodór (jako prot) i jego stabilny izotop deuter oraz niestabilny i promieniotwórczy tryt. „Zwykły” wodór (1H) czyli prot posiada jeden proton i jeden elektron, nie ma neutronów w jądrze. Deuter (2H) ma po jednym protonie i neutronie oraz jeden elektron. Tryt (3H) ma dwa neutrony, jeden proton oraz jeden elektron i w czasie około 12,32 lat rozpada się na hel.
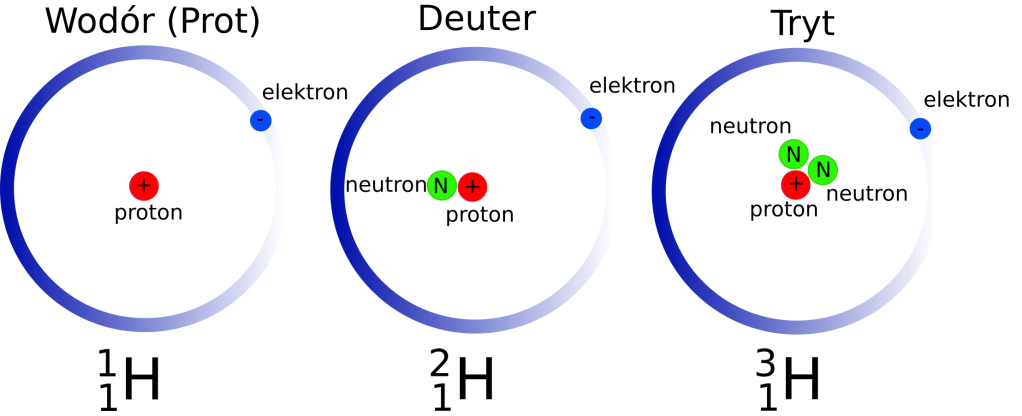
Schematyczny rysunek izotopów wodoru. Źródło: E. Pronin wzorowane na Wikipedia
W badaniach przy użyciu technik związanych z izotopami stabilnymi przyrównuje się otrzymane wyniki izotopowe danych pierwiastków, np. jakiegoś materiału lub substancji do standardowych materiałów, co pozwala na określenie czy dany sygnał izotopowy materiału, który badamy jest w „normie” czy może istnieją jakieś rozbieżności. Co ciekawe te rozbieżności, w zależności do czego wykorzystujemy analizy składu stabilnych izotopów, mogą mieć szereg interesujących zastosowań. Podobne porównania stosuje się wykorzystując inne techniki laboratoryjne (o czym napiszę innym razem). Pamiętam z konferencji o aplikacyjnych zastosowaniach badań nad składem stabilnych izotopów różnych pierwiastków dwa świetne wystąpienia. Prezentowały one ciekawe zastosowanie analiz składu stabilnych izotopów. Pierwsze dotyczyło izotopów siarki, strontu i tlenu. Drugie dotyczyło natomiast izotopów azotu. Dzięki izotopom siarki, strontu i tlenu wykazano fakt, że część rzeźb będących w posiadaniu różnych muzeów, w tym Luwru w Paryżu, nie pochodziła z miejsc z których pierwotnie przypisano ich pochodzenie. Stąd nawet podejrzewano ich podrobienie. Dowiedziono tego porównując skład izotopowy siarki, strontu i tlenu w materiale, z którego były wykonane te rzeźby czyli alabastru. Poszczególne rzeźby poddane badaniu korespondowały lub nie z alabastrem z danego miejsca jego wydobycia, obróbki i okresu, w którym to miało miejsce. Podsumowując skład stabilnych izotopów może być unikalny jak odcisk palca (podaje link do artykułu po angielsku opisujące w popularnonaukowy sposób te zagadnienia oraz publikacja, związana z tym wystąpieniem, która ukazała się 4 lata po wspomnianej konferencji Kloppmann i in. 2017).
Drugie wystąpienie, które zapadło mi w pamięć, dotyczyło podrabiania win. Analogicznie jak w sytuacji z rzeźbami, wina z danego regionu z uwagi na specyficzny typ winogron użyty do ich produkcji charakteryzują się specyficznym składem izotopów stabilnych azotu. Podróbki miały zdecydowanie inny skład stabilnych izotopów azotu, co świadczyło o tym, że na pewno nie pochodzą z danej winnicy (nie mam dostępu obecnie do książki abstraktów z konferencji, wiec wstawiam link do przykładowych badań tego typu Geana i in. 2016).
W badaniach, w których uczestniczyłem wraz z zespołem, wykazałem m.in., że dwa gatunki ramienic (ramienica omszona – Chara tomentosa L. i ramienica krucha Chara globularis Thuill.) mogą się różnić składem izotopowym węgla zarówno materii organicznej jak i wytrącanych na powierzchni ich plech węglanów. Wpływać na to może skład izotopowy nieorganicznego węgla rozpuszczonego w wodzie i różnice w typie zajmowanych siedlisk przez te dwa gatunki ramieic. Z uwagi na różnice w ekologii tych gatunków mogą one mieć również odmienne strategie pobierania dwutlenku węgla do procesu fotosyntezy. Można więc przypuszczać, iż ma to duże znaczenie dla zaobserwowanych różnic w sygnałach izotopowych (Pronin i in. 2016). Wspomnianą publikację postaram się omówić bardziej szczegółowo w kolejnym wpisie.
